推荐等级:
发布时间: 2022-04-14 11:43
扫码用手机做题
将0.72g草酸亚铁(FeC2O4)放在一个可称量的敞口容器中高温焙烧,500~600℃时,容器中的固体质量保持0.4g不变。所得物质的化学式为( )
本题解析:
【分析】根据反应前后铁元素的质量不变,确定所得物质中铁元素和氧元素的质量比,进而确定其化学式。
【解答】解:0.72g草酸亚铁中含铁元素的质量为
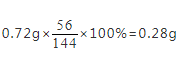
,而反应后固体质量为0.4g,不可能是铁单质,结合选项可知,应为铁的氧化物,铁元素和氧元素的质量比为0.28g:(0.4g﹣0.28g)=7:3,设铁的氧化物的化学式为FexOy,56x:16y=7:3,则x:y=2:3,故所得物质的化学式为Fe2O3。
故选:C。
【点评】本题难度不大,明确反应前后铁元素的质量不变、化学式的有关计算是正确解答本题的关键。
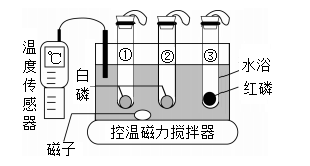
利用如图装置进行燃烧条件的探究。试管①中充满氮气,试管②③中充满氧气,升温至40℃,仅观察到②中的白磷燃烧。下列叙述错误的是( )
本题解析:
【分析】根据化学反应的原理、燃烧的条件以及实验现象来分析。
【解答】解:A、实验①白磷不燃烧是因为白磷不接触氧气,实验②中白磷能与氧气接触能燃烧,所以对比实验①②可验证燃烧需要氧气,故A正确;
B、实验③中红磷不燃烧是因为温度为达到着火点,对比实验②③可推知着火点高低:红磷>白磷,故B正确;
C、可燃物的着火点是物质固有的属性,一般不能改变,故C错误;
D、①③两支试管内的白磷和红磷均未反应,可回收再利用,故D正确。
故选:C。
【点评】本考点是用白磷探究燃烧的条件,属于实验方法和过程的探究。这类探究实验要具体问题具体分析,根据设计的步骤中不同的现象去思考、去探究,从而回答题目给出的问题。本考点主要出现在填空题和实验题中。
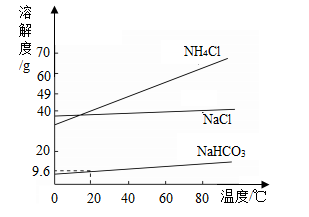
“侯氏制碱法”生产纯碱的主要反应是NaCl+NH4HCO3═NaHCO3↓+NH4Cl。如图是三种物质的溶解度曲线。下列叙述正确的是( )
本题解析:
【分析】根据固体的溶解度曲线可以知道:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性;②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小;③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。根据题目信息和溶解度曲线可知:氯化铵、氯化钠、碳酸氢钠三种固体物质的溶解度,都是随温度升高而增大,而氯化钠的溶解度随温度的升高变化比较小。
【解答】解:A、由溶解度曲线可知,0℃时,NH4Cl的溶解度小于NaCl的溶解度,故A错;
B、因为20℃时,NH4Cl的溶解度大于NaHCO3的溶解度,所以20℃时,NaHCO3饱和溶液中溶质的质量分数不一定大于NH4Cl不饱和溶液中溶质的质量分数,故B错;
C、20℃时,NaHCO3的溶解度是9.6g,即在该温度下,100g水中最多溶解9.6gNaHCO3,5.85g NaCl和7.9g NH4HCO3反应能生成8.4gNaHCO3,所以20℃时,100g水中加入5.85g NaCl和7.9g NH4HCO3固体,得到NaHCO3的不饱和溶液,不能析出NaHCO3晶体,故C错;
D、NH4Cl溶解度受温度影响较大,NaCl的溶解度受温度影响较小,所以NH4Cl固体中含有少量的NaCl,可用降温结晶的方法提纯NH4Cl,故D正确。
故选:D。
【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和结晶的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.
下列叙述正确的是( )
本题解析:
【分析】A、根据高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,进行分析判断。
B、工业上分离液态空气制取氧气的原理,进行分析判断。
C、根据自然界中植物通过光合作用的原理,进行分析判断。
D、根据人体呼出的气体的成分,进行分析判断。
【解答】解:A、该化学方程式缺少反应条件,正确的化学方程式为
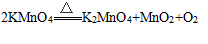 故选项说法错误。
故选项说法错误。
B、工业上分离液态空气得到O2,利用的液态氮和液态氧沸点的不同,没有新物质生成,属于物理变化,故选项说法错误。
C、自然界中植物通过光合作用吸收CO2,释放O2,故选项说法正确。
D、人体呼出的气体中CO2的含量占4.5%左右,氧气含量为16%左右,人体呼出的气体中CO2的含量比O2低的多,故选项说法错误。
故选:C。
【点评】本题难度不大,了解氧气的工业制法、光合作用的原理、人体呼出的气体的成分等是正确解答本题的关键。
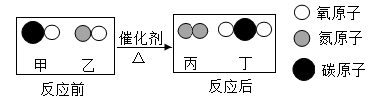
如图是甲和乙在一定条件下反应前后分子种类变化的微观示意图。下列叙述正确的是( )
本题解析:
【分析】根据甲和乙在一定条件下反应前后分子种类变化的微观示意图写出方程式,根据物质的组成、方程式的意义、物质的性质和变化等分析判断有关的说法。
【解答】解:由图可知,该反应的方程式是:

A、氧化物是由氧元素和另一种元素组成的化合物,甲为一氧化碳,属于氧化物,丙为氮气,属于单质,故A错误;
B、由方程式的意义可知,反应生成的丙与丁的分子个数比为1:2,故B错误;
C、化学反应前后原子的数目不变,故C错误;
D、该反应的反应物均为有害气体,生成物均为无害气体,所以该反应能使有害气体转化为无害物质,故D正确。
故选:D。
【点评】解决这种题的关键就是辨别分子是由何种原子构成,每种原子有几个,这样就可以得出分子的化学式,写出方程式,在对相关知识进行分析判断即可。
下列物质的性质与用途对应关系正确的是( )
本题解析:
【分析】物质的性质在很大程度上决定了物质的用途,根据常见的物质的性质和用途进行分析判断即可。
【解答】解:A、石墨质软,能在纸上留下灰黑色痕迹,所以石墨可用于制铅笔芯,并不是利用其导电性,故A错误;
B、银的导电性好,但是其价格较高,成本高,一般不用于制电线,故B错误;
C、二氧化碳的密度比空气大,且不燃烧,也不支持燃烧,所以二氧化碳可用作灭火,并不是利用其能与水反应,故C错误;
D、熟石灰的溶液显碱性,能与土壤中的酸性物质反应,所以可用于改良酸性土壤,故D正确。
故选:D。
【点评】本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键。
丙氨酸(C3H7O2N)是一种常见的氨基酸。下列叙述正确的是( )
本题解析:
【分析】A.根据有机物与无机物的概念来分析;
B.根据物质分类来分析;
C.根据分子结构来分析;
D.据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析。
【解答】解:A、丙氨酸(C3H7O2N)是一种含碳元素的化合物,属于有机小分子化合物,说法正确;
B、丙氨酸是一种常见的氨基酸,氨基酸是蛋白质的基本组成单位,不是蛋白质,说法错误;
C、分子是由原子构成的,每个丙氨酸分子中含有2个氧原子,不含氧分子,说法错误;
D、丙氨酸中碳、氢元素的质量比为12×3:(1×7)=36:7,说法错误;
故选:A。
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力。
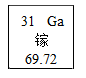
1875年,布瓦博德朗利用光谱分析在闪锌矿中发现了镓,门捷列夫预言的“类铝”元素得到了证实。如图是镓元素在元素周期表中的信息。下列叙述错误的是( )
本题解析:
【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】解:A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是镓,带“钅”字旁,属于金属元素,故选项说法正确。
B、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为69.72,相对原子质量单位是“1”,不是“克”,故选项说法错误。
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为31;根据原子中原子序数=核电荷数=质子数=核外电子数,则该镓原子中的质子数是31,故选项说法正确。
D、1875年,布瓦博德朗利用光谱分析在闪锌矿中发现了镓,门捷列夫预言的“类铝”元素得到了证实,镓与铝的性质相似,故选项说法正确。
故选:B。
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)是正确解答本题的关键。
下列化学用语中数字“2”表示的意义正确的是( )
本题解析:
【分析】A、标在元素符号前面的数字表示原子的个数。
B、标在化学式中元素右下角的数字表示一个分子中所含原子的数目。
C、标在分子符号前面的数字表示分子的个数。
D、标在元素符号右上角的数字表示1个离子所带的电荷数。
【解答】解:A、标在元素符号前面的数字表示原子的个数,2H中的“2”表示氢原子的个数为2,故选项说法错误。
B、标在化学式中元素右下角的数字表示一个分子中所含原子的数目,O2中的“2”表示1个氧分子中含有2个氧原子,故选项说法错误。
C、标在分子符号前面的数字表示分子的个数,2CO中的“2”表示一氧化碳分子的个数为2,故选项说法正确。
D、标在元素符号右上角的数字表示1个离子所带的电荷数,Fe2+中的“2”表示一个亚铁离子带有两个单位的正电荷,故选项说法错误。
故选:C。
【点评】本题难度不大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在。
自来水厂净水过程中不常用的方法是( )
本题解析:
【分析】根据自来水的生产过程以及所用净化水的方法来分析。
【解答】解:自来水厂净水过程中用到沉淀(除去水中较大的难溶性杂质)、过滤(除去水中的难溶性杂质)、吸附(除去水中的色素和异味)、消毒(杀灭水中的微生物)等,没有用到蒸馏操作。
故选:D。
【点评】要想解答好这类题目,首先,要熟记混合物的分离方法、水的净化方法、原理和相关实验操作等。然后结合实验情景和问题情景,细致地分析题意和实验信息,并根据所学的相关知识,选择好净化的方法,进行净化实验操作,或者是通过细心地思考、探究,来解答相关的实际问题等。
试卷分类:英语
练习次数:300次
试卷分类:语文
练习次数:282次
试卷分类:语文
练习次数:315次
试卷分类:英语
练习次数:286次
试卷分类:数学
练习次数:295次
试卷分类:语文
练习次数:279次
试卷分类:语文
练习次数:279次
试卷分类:语文
练习次数:277次
试卷分类:语文
练习次数:291次
试卷分类:英语
练习次数:363次